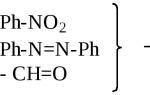Fullereenid: avastamise ajalugu ja omadused. Fullereen, selle tootmine, omadused ja rakendused Bioloogid kinnitavad hüpoteesi
Fullereenid
Sissejuhatus
§1 Fullereenid – süsiniku allotroopne modifikatsioon
1.1 Fullereenide avastamise ajalugu
1.2 Fullereenide geomeetriline struktuur
1.3 Fullereenide omadused
1.4 Fullereenid looduses
1.5 Fullereenide saamine
1.6 Fullereenide kasutamine
§2 Hulknurgad ja hulktahukad
2.1 Hulknurgad
2.2 Tavaline viisnurk
2.3 Tavalise viisnurga konstrueerimise viisid
2.4 Hulktahuka määratlus ja hulktahukate tüübid
2.5 Platoonilised tahked ained
2.6 Euleri teoreem
2.7 Aleksandrovi teoreem
2.8 Duaalsus
§3 Eraldatud viisnurkade (viisnurkade) reegel
Järeldus
Kirjandus
polüeedri aatom süsinikfulereen
Sissejuhatus
Selle essee kirjutamise teema valimisel saate määrata mitu põhjust.
Esmalt tutvusime geomeetria tundides polühedratega – abstraktsete matemaatiliste kujunditega. Polüeedreid uurides tekkis meil huvi, kuidas sellised objektid looduses ilmuvad. Teiseks tutvusime keemiatundides süsiniku allotroopia fenomeni uurides põgusalt ebatavaliste molekulidega - fullereenidega.
Fullereenid on keemiamaailmas üsna uus mõiste. Nad on väga huvitavad, fullereenide omadused on väga mitmekesised, fullereeni molekuli struktuuri poolest on nad polüeedrid. Kirjanduse esialgne analüüs näitas, et fullereenide omaduste ja struktuuri kohta pole palju materjali, see on väga hajutatud. Seetõttu tuli meil analüüsida palju materjali, mis oli seotud nii töö matemaatilise kui ka keemilise osaga.
Eesmärk:
Uurige fullereeni molekulide näitel, kuidas avalduvad polüeedrite omadused.
Ülesanded:
1) defineerida fullereene;
2) kirjeldab lühidalt fullereenide ehitust ja omadusi;
3) defineerib hulknurgad ja hulktahukad;
4) määrab hulknurkade ja hulktahukate tüübid;
5) Mõelge fullereeni molekulide näitel, mis tüüpi polüeedreid esineb
6) Mõelge, kuidas on fullereenide stabiilsus seotud nende geomeetrilise struktuuriga.
§1 Fullereenid – süsiniku allotroopne modifikatsioon
Praegu kasutatakse mõistet "fullereenid" laiale polüaatomiliste süsiniku molekulide klassile Cn, kus n = 60. Nendest molekulidest moodustunud tahkeid aineid nimetatakse tavaliselt fulleriitideks. fullereen on süsiniku kolmas allotroopne vorm (esimesed kaks on teemant ja grafiit). Fullereeni molekul on orgaaniline molekul ja fullereen ise on molekulaarne kristall, mis on ühenduslüli orgaanilise ja anorgaanilise aine vahel.
1.1 Fullereenide avastamise ajalugu
1973. aastal avaldasid Venemaa teadlased D. A. Bochvar ja E. N. Galpern kvantkeemiliste arvutuste tulemused, millest järeldub, et molekulis peaks olema stabiilne süsiniku vorm, mis sisaldab 60 süsinikuaatomit ja millel ei ole asendajaid. Samas artiklis pakuti välja sellise hüpoteetilise molekuli vorm. Selle töö järeldused tundusid tol ajal täiesti fantastilised. Keegi ei osanud ette kujutada, et selline molekul võiks eksisteerida ja veelgi enam – kuidas selle tootmist enda peale võtta. See teoreetiline töö oli oma ajast mõnevõrra ees ja unustati alguses lihtsalt.
1980. aastatel võimaldasid astrofüüsikalised uuringud kindlaks teha, et mõnede tähtede, nn "punaste hiiglaste" spektris leiti ribasid, mis viitavad erineva suurusega puhaste süsiniku molekulide olemasolule.
1985. aastal G. Kroto. Ja R. Smalley hakkas uurimistööd läbi viima juba "maistes" tingimustes. Nad viisid läbi uuringud, mis näitasid suurte süsinikuaatomite - C 60 ja C 70 - olemasolu. Selle tulemusena pakuti välja viisnurkadest ja kuusnurkadest kokkupandud hulktahuka struktuur. See oli Bochvari poolt 12 aastat tagasi pakutud struktuuri täpne kordus.
Nimetus "fullereen" anti kuulsa Ameerika arhitekti Buckminster Fulleri auks, kes tegi ettepaneku ehitada ažuursed kuppelkonstruktsioonid viie- ja kuusnurga kombinatsiooniga (joonis 2 ja 3). Esmapilgul tundub, et struktuur on kokku pandud kolmnurkadest, kuid viie- ja kuuekiireliste tsentrite vaheldumine vastab just fullereeni struktuurile.
1.2 Fullereenide geomeetriline struktuur
Kõige üldisemal kujul on fullereeni molekulid polühedron, mis on ehitatud kahte tüüpi hulknurkadest: kuusnurgad (kuusnurgad) ja viisnurgad (viisnurgad). Kõikide hulknurkade tipud on süsinikuaatomid. Hulknurkadest koosneva hulktahuka pind järgib Euleri valemit.
Siit järeldub, et fullereen peab sisaldama 12 viisnurka ja suvalise arvu kuusnurki. Tõepoolest, kõigil saadud või simuleeritud fullereenidel on 12 "kohustuslikku" viisnurka. Sõltuvalt kuusnurkade arvust võib sfääriliste molekulide koostis olla erinev. Lihtsaim fullereen on teoreetiliselt valemiga C 20 ja koosneb vaid 12 viisnurgast, moodustades korrapärase hulktahuka – dodekaeedri (joonis 4). Sellise molekuli ebastabiilsuse tõttu oli aga fullereen-20 eraldamine peaaegu võimatu.
Olemasolevate seisukohtade kohaselt fullereenide struktuuri kohta võivad stabiilsed olla ainult need fullereenid, milles 12 "kohustuslikku" viisnurka on eraldatud kuusnurkadega ja millel ei ole ühiseid tippe ega servi. Enim uuritud fullereen C 60 on kärbitud ikosaeedri kujuga ja selle välise sarnasuse tõttu jalgpallipalliga nimetatakse seda sagedamini jalgpallifulereeniks (joonis 5). C 60 molekulil on 32 tahku (12 viisnurka ja 20 kuusnurka).
Kõrgemad fullereenid (näiteks C 78 või C 80) võimaldavad viisnurkade ja kuusnurkade kaupa pinna "väljapaneku" erinevas järjekorras, säilitades samal ajal nende koguarvu ja viisnurkade eraldamise põhimõtte, s.t. sisaldavad isomeere.
1.3 Fullereenide omadused
Fullereenid moodustavad molekulaarseid kristalle – fulleriite. Nende struktuur ja füüsikalis-keemilised omadused on hästi uuritud. Kristallvõre C 60 on näokeskne kuup, igal molekulil on 12 "naabrit", molekulid on omavahel nõrgalt seotud. Sellist molekulaarvõret iseloomustavad madalad sublimatsioonitemperatuurid (800 °C) ja C 60 molekulid lähevad aurudesse. mis täiuslikult "elavad" gaasifaasis kuni temperatuurini 1500 K
Fullerite C60 on sinepivärvi tahke aine. C70 on punakaspruun tahke aine.
Fulleriidid lahustuvad orgaanilistes lahustites. Tuntumad lahustid võib järjestada fulleriidi lahustuvuse vähenemise järjekorras: süsinikdisulfiid, tolueen, benseen, süsiniktetrakloriid, dekaan, heksaan, pentaan.
C60 proovid on hapniku puudumisel tundlikud ultraviolettkiirguse suhtes ja võivad osaleda lagunemisreaktsioonides. Seetõttu tuleks neid hoida pimedas ja vaakumis või lämmastiku all.
Puhas fullereen toatemperatuuril on väga madala juhtivusega isolaator või pooljuht.
Leelismetalli fulleriidid koostisega A 3 C 60 muutuvad ülijuhtivaks temperatuuril alla teatud väärtuse
Fullereenidel on erinevad magnetilised omadused.
Kristallilistel fulleenidel on fotojuhtivus. Nähtava valgusega kiiritades fulleriidi kristalli elektritakistus väheneb. Fotojuhtivust ei oma mitte ainult puhas fulleriit, vaid ka selle erinevad segud.
Fullereene hõlmavate protsesside uuringute tulemused näitavad nende anomaalselt kõrget stabiilsust. Veelgi enam, ühtlaste süsinikuaatomite väärtustega molekulide stabiilsus nületab oluliselt paaritute väärtustega molekulide stabiilsust n. C-molekulide jaoks n (n-paaritu) kõige tõenäolisem on süsinikuaatomi elimineerimine, seega paaritute klastrite osa n ei ületa 1%. Katsed näitavad, et tahke C60 fullereen sublimeerub 400°C juures lagunemata.
Fullereeni molekulidel on kõrge elektronegatiivsus ja nad on võimelised enda külge kinnitama kuni kuus vaba elektroni. See muudab need võimsateks oksüdeerivateks aineteks, mis on võimelised moodustama palju uusi huvitavate uute omadustega keemilisi ühendeid. See fullereenide omadus avastati juba ühes esimestest nende keemilise muundamise katsetest, kus viidi läbi C60 hüdrogeenimine. Selle reaktsiooni saadus oli C60H36 molekul.
Fullereenid on lihtaineteks lagunemise protsessi suhtes keemiliselt väga inertsed: C 60 molekul püsib stabiilsena inertses atmosfääris kuni 1700 K. Hapniku juuresolekul aga täheldatakse oksüdeerumist palju madalamatel temperatuuridel (umbes 500 K). Sel juhul moodustub amorfne struktuur, milles C 60 molekuli kohta on 12 hapnikuaatomit. Temperatuuri tõusuga kaasneb C 60 molekuli kuju kaotus.
1.4 Fullereenid looduses
Fullereenide avastamine tõi kaasa ka fullereenstruktuuride otsimise süsiniku sisaldavates kivimites.
Loodusest on leitud fullereene. Sarnase jahmatava avastuse tegid ka geokeemikud. Nad leidsid fullereeni olemasolu proovides, mis koguti Sadburi kraatri setetest, mis tekkisid 1,85 miljardit aastat tagasi meteoriidi kokkupõrkest. Paralleelsete ja sõltumatute uuringute käigus on fullereene leitud ka Uus-Meremaa kriidiajastu-tertsiaari piirilt pärit proovidest. Fullereenide esinemine setetes on seletatav asjaoluga, et umbes 65 miljonit aastat tagasi puhkes Maal hiidmeteoriidi löögi tagajärjel võimas tulekahju, mis aitas kaasa selliste struktuuride tekkele.
On teada, et šungiitkivim tekkis umbes 2 miljardit aastat tagasi ja sisaldab mittekristallilist süsinikku, mikroelemente, mineraale, vähesel määral orgaanilist ainet ja vett. Süsinikusisaldus, mis määrab šungiitkivimite peamised omadused, jääb vahemikku 1–70%, kuid mõnel pool võib see ulatuda 98%-ni. Elektronmikroskoopilised uuringud on näidanud, et kõiki proove iseloomustab üks põhiline struktuurielement – 10 nm suurused süsinikkuulikesed, mille sees tuvastati tühimike olemasolu. Samuti tuvastati šungiidi süsiniku (SHC) ja fullereenide grafiiditaoliste kihtide moonutuste sarnasus. Nende andmete põhjal pakkusid autorid välja SHU jaoks fullereenilaadse struktuuri. Läbiviidud katsed näitasid C60 ja C70 fullereenide esinemist koguses 0,0001%. Selle põhjal pakuti välja šungiit süsiniku fullereeni mudel.
1.5 Fullereenide saamine
Fullereeni struktuur on lähedane grafiidi omale, seega on kõige tõhusam viis nende saamiseks grafiidi termilisel aurustamisel kas grafiitelektroodi oomilise kuumutamise või laserkiirguse tulemusena. Grafiidi mõõdukal kuumutamisel hävivad üksikute kihtide vahelised sidemed ja fullereenid monteeritakse kuusnurkse konfiguratsiooniga fragmentidest. Saadud kivisöe kondensaat koos C-60 ja C-70 klastritega sisaldab suurt hulka väiksemaid molekule, millest märkimisväärne osa läheb C 60 ja C 70, kui seda hoitakse mitu tundi temperatuuril 500–600 ° C või temperatuuril madalam temperatuur mittepolaarses lahustis.
Lisaks ülaltoodud fullereenide saamise meetoditele, mis on süsinikku sisaldavate ainete termilised lagunemisprotsessid, on välja töötatud katalüütiline meetod fullereenide sünteesiks kivisöetõrvast. Selle meetodi eripäraks on protsessi madal temperatuur, mis on 200–400 ° C. See on suurusjärgu võrra madalam kui grafiidi termilise lagunemise temperatuur (3300 ° C)
1.6 Fullereenide kasutamine
On väljavaade kasutada fullereene ülikõrge infotihedusega mälukandja loomise alusena. Kui kasutada infokandjatena fullereenmagnetkettaid, mis asuvad kõvaketta pinnal 5 nm kaugusel. üksteisest, siis saavutab salvestustihedus väärtuse 4 * 10 12 bitti / cm. 2. On tehtud ettepanek võtta akude tootmise alusena fullereeni. Käsitletakse nende kasutamise küsimusi fotodetektorite ja optoelektrooniliste seadmete, ravimite ja ülijuhtivate materjalide loomisel. Tuntud meetod teemantide saamiseks polükristallilisest fulleriidist.
§2 Hulknurgad ja hulktahukad
2.1 Hulknurgad
Hulknurk- geomeetriline kujund tasapinnal, mis on piiratud suletud katkendjoonega; sirge, mis saadakse, kui võtta n suvalist punkti A 1, A 2, ..., A n ja ühendada igaüks neist järgmisega, viimane aga esimesega, sirgjoonelõikudega.
Hulknurki on kahte tüüpi: kumer ja mittekumer. Vaatleme lähemalt kumeraid hulknurki. Hulknurk kutsus kumer kui hulknurga ükski külg, olles piiramatult pikendatud, ei lõika hulknurka kaheks osaks. Kumerad hulknurgad on korrapärased ja ebakorrapärased, kuid me kaalume õigeid. Kumer hulknurk helistas õige kui kõik küljed on võrdsed ja kõik nurgad on võrdsed. Korrapärase hulknurga keskpunkt on punkt, mis on võrdsel kaugusel kõigist selle tippudest ja külgedest.
Korrapärase hulknurga kesknurk on nurk, mille all on nähtav külg selle keskpunktist. Regulaarse hulknurga omadused:
1) Regulaarne hulknurk on kirjutatud ringi ja ümbritsetud ringiga, kusjuures nende ringide keskpunktid langevad kokku;
2) Korrapärase hulknurga keskpunkt langeb kokku sissekirjutatud ja piiritletud ringide keskpunktidega;
3) Parem pool n-gon on seotud raadiusega R piiritletud ringi valem;
4) Perimeetrid õige n-gonid on seotud piiritletud ringide raadiustena.
5) Korrapärase n-nurga diagonaalid jagavad selle nurgad võrdseteks osadeks.
2.2 Tavaline viisnurk
Vaatleme üksikasjalikumalt tavalisel viisnurgal - viisnurgal.
Põhisuhted: nurk viisnurga tipus on 108°, välisnurk 72°. Viisnurga külgi väljendatakse sissekirjutatud ja piiritletud ringide raadiustena:
Ehitame tavalise viisnurga. Piiratud ringiga on seda lihtne teha. Selle keskelt tuleb järjestikku kõrvale jätta nurgad, mille tipp on ringi keskel, mis on võrdne 72 °. Nurkade küljed lõikuvad ringi viies punktis, ühendades need järjestikku, saame tavalise viisnurga. Ja nüüd joonistame kõik diagonaalid sellesse viisnurka. Need moodustavad korrapärase tähtkujulise viisnurga, st. kuulus pentagramm. Huvitaval kombel moodustavad pentagrammide küljed, lõikuvad, jälle korrapärase viisnurga, mille diagonaalide lõikumine annab meile uue pentagrammi ja nii edasi lõpmatuseni (vt joonis 6).
Pentagramm on tavaline mittekumer viisnurk, see on ka tavaline tähtviisnurk või tavaline viisnurkne täht. Paljud lilled, meritähed ja siilid, viirused jne on viieharulise tähe kujuga. Pentagrammi esimene mainimine viitab Vana-Kreekale. Kreeka keelest tõlgituna tähendab pentagramm sõna-sõnalt viit rida. Pentagramm oli Pythagorase koolkonna (580–500 eKr) tunnus. Nad uskusid, et sellel kaunil hulknurgal on palju müstilisi omadusi. Aupaklik suhtumine pentagrammi oli omane ka keskaegsetele müstikutele, kes laenasid palju pütagoorlastelt. Keskajal usuti, et pentagramm toimib Saatana turvamärgina.
2.3 Tavalise viisnurga konstrueerimise viisid
Huvi pakub tavalise viisnurga ligikaudne ehitus. A. Durer see viiakse läbi tingimusel, et kompassi lahendus on muutumatu, mis suurendab konstruktsiooni täpsust (joon. 7).
Ehitamise meetodit kirjeldab Durer järgmiselt: "Kuid viisnurk, mis on ehitatud kompassi muutumatu lahendusega, tehke seda. Joonistage kaks ringi nii, et igaüks neist läbiks teise keskpunkti Ühendage kaks keskpunkti A ja B sirgjoonega. Sellest saab viisnurga külg. Ringide lõikepunktid tähistavad ülalt C, alt D ja tõmmake sirgjoon CD. Pärast seda võtke muutmata lahendusega kompass ja määrake üks selle jalad punktis D, tõmmake teine läbi mõlema tsentri A ja B, kuni see lõikub mõlema ringiga. Määrake lõikepunktid punktidega E ja F ning märkige lõikepunktiks joonega CD G. Nüüd tõmmake sirgjoon läbi E ja G, kuni see lõikub ringjoonega. Märkige see punkt kui H. Seejärel tõmmake veel üks joon läbi F ja G, kuni see lõikub ringjoonega ja asetage siia J. J,A ja H,B ühendamine sirgjoontega, saame viisnurga kolm külge. Arvestades võimalust, et selle pikkusega kaks külge jõuavad punktidest J ja H punkti K, saame viisnurga".
Olgu w antud ring raadiusega R keskpunktiga O. Konstrueerime esmalt korrapärase kümmenurga, mis on kirjutatud ringi w. Selleks joonistame ringi w vastastikku risti raadiused OA1 ja OB ning lõigule OB nagu läbimõõdule konstrueerime ringi keskpunktiga C. Lõik A1C lõikub selle ringiga mingis punktis D. Järgmiseks märgime punktid A2, A3, ..., A10 ringil w nii, et A1A2= A2A3=….
A9A10 = A1D. Kümnenurk A1A2 ... A10 on soovitud. Tavalise viisnurga ehitamiseks peate selle kümnenurga punktid ühendama läbi ühe, mis tähendab, et ühendame punktid A1, A3, A5, A7, A9. Soovitud on viisnurk A1A3A5A7A9.
Pentagrammi küljed, mis lõikuvad, jagavad üksteist segmentideks, mille pikkused moodustavad kuldse lõike.
2.4 Hulktahuka määratlus ja hulktahukate tüübid
Nagu varem mainitud, on fullereeni molekulid polüeedrid. Vaatleme seda kontseptsiooni üksikasjalikumalt.
Milliseid kujundeid nimetatakse tavalisteks hulktahukateks? Geomeetria käigus antakse definitsioon: “Polühedron on geomeetriline keha, mis on igast küljest piiratud lamedate hulknurkadega, mida nimetatakse tahkudeks. Tahkude külgi nimetatakse hulktahuka servadeks ja servade otste nimetatakse hulktahuka tippudeks.
Tavaliste hulktahukate nimed pärinevad Vana-Kreekast. Kreeka keelest tõlkes tähendavad need: tetraeedrit, kuusnurka, oktaeedrit, dodekaeedrit ja kahekümnetahulist (joon. 10).
2.5 Platoonilised tahked ained
Regulaarseid hulktahukaid nimetatakse sageli platoonilisteks tahketeks aineteks, kuna ta mainis neid esimesena oma teaduslikes traktaatides, kuigi need olid tuntud juba ammu enne teda.
Platon (joon. 11) uskus, et maailm on ehitatud neljast "elemendist" - tulest, maast, õhust ja veest ning nende "elementide" välimus on nelja korrapärase hulktahuka kujuga. Niisiis isikustas tetraeeder tuld, kuna selle tipp on suunatud ülespoole, nagu leegi leek; ikosaeeder - kui kõige voolujoonelisem - vesi; kuubik - figuuridest stabiilseim - maa, oktaeedr - kui disainilt kõige "õhulisem" - õhk. Viies hulktahukas – dodekaeedr – kehastas "kõike olemasolevat", sümboliseeris kogu maailma ja taevast ning seda austati kui kõige olulisemat.
Korrapärane hulktahukas on hulktahukas, mille kõik tahud on võrdsed korrapärased hulknurgad ja igas tipus koondub sama arv servi.
Alustan oma kaalumist korrapärase hulktahukaga, mille tahud on võrdkülgsed kolmnurgad . Esimene neist on tetraeeder. Tetraeedris kohtuvad kolm võrdkülgset kolmnurka ühes tipus; samas kui nende alused moodustavad uue võrdkülgse kolmnurga.
Tetraeedril on platooniliste tahkete seas kõige vähem tahke ja see on lameda korrapärase kolmnurga kolmemõõtmeline analoog, millel on tavaliste hulknurkade seas kõige vähem külgi.
Järgmist keha, mille moodustavad võrdkülgsed kolmnurgad, nimetatakse oktaeedriks. Oktaeedris kohtuvad neli kolmnurka ühes tipus; tulemuseks on nelinurkse põhjaga püramiid. Kui ühendate kaks sellist püramiidi alustega, saate kaheksa kolmnurkse küljega sümmeetrilise keha - oktaeedri.
Nüüd võite proovida ühendada viis võrdkülgset kolmnurka ühes punktis. Tulemuseks on 20 kolmnurkse tahuga kujund – ikosaeedr. Järgmine õige hulknurga kujund on ruut . Kui ühendame kolm ruutu ühes punktis ja seejärel lisame veel kolm, saame täiusliku kuuetahulise kujundi, mida nimetatakse kuubiks. Lõpuks on veel üks võimalus korrapärase hulktahuka konstrueerimiseks järgmise korrapärase hulknurga, viisnurga kasutamise põhjal. Kui koguda 12 viisnurka nii, et igas punktis kohtuvad kolm viisnurka, saame teise platoonilise tahkise, mida nimetatakse dodekaeedriks.
Järgmine korrapärane hulknurk on kuusnurk. Kui aga ühendada kolm kuusnurka ühes punktis, siis saame pinna ehk kuusnurkadest on võimatu kolmemõõtmelist kujundit ehitada. Ükski teine korrapärane hulknurk, mis asub kuusnurga kohal, ei saa üldse moodustada tahkeid osakesi. Nendest kaalutlustest järeldub, et on ainult viis korrapärast hulktahukat, mille tahud võivad olla ainult võrdkülgsed kolmnurgad, ruudud ja viisnurgad.
Vaatleme kahte teoreemi pindadena käsitletavate kumerate hulktahukate üldteooriast.
2.6 Euleri teoreem
Tabelis 1 on toodud tavaliste hulktahukate tahkude, tippude ja servade arvu suhe.
Tabel number 1.
Arvestades tabelit number 1, esitame endale küsimuse: "Kas iga veeru arvude suurenemises on muster?" Ilmselt mitte. "Servad" veerus jälgitakse algul mustrit (4+2=6, 6+2=8), seejärel kaob muster (8+2?12, 12+2?20). "Tippude" veerus pole isegi stabiilset tõusu. Tippude arv kas suureneb (4-lt 8-le, 6-lt 20-le) ja seejärel väheneb (8-lt 6-le, 20-lt 12-le). Veerus "ribid" pole mustreid isegi näha. Kuid ärgem andkem alla. Lõppude lõpuks võrdlesime numbreid samas veerus. Kuid võite arvestada kahe veeru arvude summaga, vähemalt veergudes "pinnad" ja "tipud" (D ja C). Seejärel teeme uue arvutuste tabeli.
Tabel number 2.
Nüüd on muster palja silmaga nähtav. Sõnastame selle järgmiselt: "Tahkude ja tippude arvu summa võrdub kahe võrra suurendatud servade arvuga." Niisiis, oleme tõestanud Euleri teoreemi (1752). (Tippude arv miinus servade arv pluss kumera hulktahuka tahkude arv on võrdne kahega). Nagu eespool mainitud, on lihtsaim C 20 fullereen dodekaeedr, see tähendab, et selle kohta kehtib Euleri teoreem. Kõige stabiilsema C 60 fullereeni molekulil on 60 tippu, 32 tahku ja 90 serva, see tähendab 60 - 90 + 32 = 2, see tähendab, et ka Euleri teoreem on täidetud.
2.7 Aleksandrovi teoreem
Järgmine teoreem on Aleksandrovi teoreem (1939): See teoreem on olemasoluteoreem, see tähendab, et see näitab, milliste arengutega kumerad hulktahukad eksisteerivad. Selleks, et muuta arendus kumera hulktahuka pinnaks, on vajalik, et: a) oleks täidetud Euleri tingimus ja b) et ühes tipus liimimisel koonduvate tasapindade nurkade summa oleks väiksem kui 360°. mis tahes tipu jaoks.
Joonisel 12 on kujutatud tasapinnalised skaneeringud kolmest kuulsaimast fullereenist: C 60 , C 70 ja C 84 (meenutab pesapalli, selguse huvides on pall joonisel õmmeldud). Ruumilise mudeli liimimisel suurendatakse esmalt arendust nii, et polüeedri servade pikkus on 2-3 cm Seejärel lõigatakse arendus mööda perimeetrit. Punktiga tähistatud tipu küljelt lõigatakse kuusnurgad numbriga "5" ja need eemaldatakse. Kuusnurgad tähega "T" - liimimiseks mõeldud keeled. Kui mudel on kokku liimitud, moodustuvad numbriga “5” kuusnurkade asemel viisnurgad (väljalõigatud).
Kui arvestada fullereeni molekulide lahtivoltimist (joonis 8), siis näeme, et 2 kuusnurka ja viisnurk koonduvad vastava kujundi tipus (siis võrdub lamenurkade summa vastavalt 120 0 +120 0 +72 0 = 312 0<360 0). То есть выполняется второе условие теоремы Александрова.
2.8 Duaalsus
Kõigi tavaliste hulktahukate vahel on hämmastavad geomeetrilised ühendused. Nii näiteks on kuup ja oktaeeder duaalsed, st saadakse üksteisest, kui ühe tahkude raskuskeskmed võetakse teise tippudeks ja vastupidi. Samamoodi on ikosaeeder ja dodekaeedr duaalsed.
Tetraeeder on iseendaga duaalne. Dodekaeedr saadakse kuubist, ehitades selle külgedele "katused", tetraeedri tipud on kuubiku suvalised neli tippu, mis ei külgne paarikaupa mööda serva, st kõik muud korrapärased hulktahukad on võimalik saada kuubist. . Tuleb märkida, et kahe polüheedri paari puhul on ühe tippude arv võrdne teise tahkude arvuga ja nende servad on võrdsed. Kahekordsed hulktahukad on näidatud joonisel 13.
§3 Eraldatud viisnurkade (viisnurkade) reegel
Stabiilsuse poolest võib fullereene jagada kahte tüüpi: stabiilsed ja ebastabiilsed.
Nende vaheline joon võimaldab meil tõmmata isoleeritud viisnurkade reegli (Isolated Pentagon Rule, IPR). See reegel ütleb, et kõige stabiilsemad on need fullereenid, mille viisnurgad ei puutu üksteisega kokku, see tähendab, et iga viisnurk on ümbritsetud viie kuusnurgaga ja tal on ühised servad ainult kuusnurkadega. Buckminsterfullereen on fullereenide esimene esindaja, mis rahuldab isoleeritud viisnurkade reeglit, C 70 on teine esindaja.
C 60 molekulis, mis on fullereeni perekonna kõige sümmeetrilisem esindaja, on kuusnurkade arv 20. Sel juhul piirneb iga viisnurk ainult kuusnurkadega ja igal kuusnurgal on kolm ühist külge kuusnurkadega ja kolm viisnurkadega.
Fullereenidel, mille n > 70, on alati isomeer, mis järgib intellektuaalomandi õiguste reeglit, ja selliste isomeeride arv kasvab kiiresti. Leiti 5 C 78 jaoks, 24 C 84 ja 40 C 90 jaoks. Kõigil teistel fullereenidel, mille n on vahemikus 22 kuni 68, on üksteisega külgnevad viisnurgad ja need on vähem stabiilsed. Kuid hoolimata sellest reeglist oli võimalik saada must kile paksusega umbes 100 nm, mis koosneb peamiselt C 36 molekulidest. Iga molekul on moodustatud 12 viisnurksest ja kahest kuusnurksest süsiniku ringist ning sellel on kuuendat järku sümmeetriatelg.
Fullereenide uurimise arenedes sünteesiti ja uuriti fullereeni molekule, mis sisaldavad erinevat arvu süsinikuaatomeid, 36 kuni 540. Küll aga tekkis küsimus olemasolu võimalikkusest ja võimalikult väikse fullereeni molekuli C 20 saamise meetodist. , on ikka veel lahendamata. Sellise molekuli pind peaks koosnema ainult viisnurkadest ja mitte sisaldama üldse kuusnurki. Sellist struktuuri iseloomustavad palju teravamad nurgad kui suurte fullereeni molekulide omad ja see ei allu isoleeritud viisnurkade reeglile, mistõttu oli põhjust kahelda keemilises stabiilsuses ja sellest tulenevalt ka C 20 molekuli saamise võimaluses. Samas ilma C20ta nägi fullereeniperekond välja puudulik.
Järeldus
Käesolevas artiklis käsitlesime fullereenide – fullereenide – mõistet – suhteliselt hiljuti avastatud süsiniku allotroopset modifikatsiooni. Erinevalt teistest süsiniku allotroopsetest modifikatsioonidest on fullereenidel molekulaarne struktuur ja molekulid on poolregulaarsed hulktahukad. Fullereenid on matemaatikas uuritud abstraktsete kujundite – hulktahukate ja hulknurkade – ilming looduses. Fullereenid on ained, millel on suured väljavaated kasutada erinevatel eesmärkidel, mistõttu on nende geomeetrilise struktuuri uurimine ja uurimine väga oluline.
Fullereeni molekulide struktuuri arvestades jõudsime järeldusele, et need järgivad kumerate hulktahukate jaoks sõnastatud teoreemi: Euleri teoreem ja Aleksandrovi teoreem.
Kirjandus
1. Zolotukhin I. V., Fulleriit - süsiniku uus vorm, Sorsovsky Educational Journal, nr 2, 1996, lk. 51-56.
2. Sidorov L. N., Gaasiklastrid ja fullereenid, Sorsovsky Educational Journal, nr 3, 1998, lk. 65-71.
3. Keemia koolis, nr 1, 2001, UURINGUD, AVAStused, ENNUSTUSED: Fullereen C36
4. Belov D. V., SÜSIKU uued polümorfsed MUUDATUSED, Keemia koolis, nr 2, 2003.
5. Semenov E. E. Geomeetriaõpiku lehekülgede taga, M, Valgustus, 1999.
6. Ryvkin A., A, Ryvkin A. Z., Matemaatika käsiraamat, M, Kõrgkool, 1987
7. Atanasyan L. S., Geomeetria 7-9, M., Valgustus, 2005.
8. Sharygin I. F., Geomeetria 7-9, M., Bustard, 2002.
Sarnased dokumendid
Süsiniku nanostruktuuride struktuur. Avastamise ajalugu, geomeetriline struktuur ja fullereenide saamise meetodid. Nende füüsikalised, keemilised, sorptsiooni-, optilised, mehaanilised ja triboloogilised omadused. Fullereenide praktilise kasutamise väljavaated.
kursusetöö, lisatud 13.11.2011
Grafeeni ehituslikud iseärasused – ühekihiline kahemõõtmeline süsiniku struktuur, selle vead ja omadused. Grafeeni võimalikud rakendused. Fullereenide struktuur ja tootmine. Süsiniknanotorude klassifitseerimine kihtide arvu järgi, nende kasutamine.
kursusetöö, lisatud 03.03.2015
Fullereenid on süsiniku uued allotroopsed vormid: kristallvõre struktuur, elektrooniline struktuur ja keemilised omadused. Fullereenide uuringud, nende kasutamise väljavaated bioloogias ja meditsiinis. Vees lahustuva vormi saamise meetodid - fullerenoolid.
abstraktne, lisatud 09.12.2012
Kroonieetrite ja fullereenide ehitus ja omadused, nende valmistamine ja kasutamine. Paigaldusskeem monokihtide saamiseks, lahuste valmistamine ja p-A isotermide konstrueerimine. Molekuli modelleerimine ja molekuli poolt hõivatud ala määramine ujuvas kihis.
lõputöö, lisatud 01.04.2011
Fullereen kui süsiniku allotroopsete vormide klassi kuuluv molekulaarne ühend, tootmismeetodid. Tutvumine fullereenidel põhinevate ühendite mitmesuguste füüsikalis-keemiliste ja struktuuriliste omadustega. Fullereeni sisaldavate segude kasutusvaldkondade analüüs.
abstraktne, lisatud 18.10.2013
Fulleriit kui suurte süsiniku molekulide kristall Cn-fullereenid. Tutvumine nanokristalliliste materjalide põhiomadustega, eeliste analüüs: kõrge viskoossus, suurenenud kulumiskindlus. Nanomaterjalide mehaaniliste omaduste iseloomustus.
abstraktne, lisatud 20.05.2014
Konstantse elektrivälja mõju mustrid polütsükliliste aromaatsete süsivesinike, tahma, fullereenide saagisele benseeni-hapniku leegis sõltuvalt elektroodidevahelise kauguse muutumisest, elektroodisüsteemi tüübist, väljatugevusest.
lõputöö, lisatud 16.06.2013
Nanotehnoloogia põhimõisted ja nanokeemia areng. Süsiniku roll nanomaailmas. Fullereenide kui süsiniku olemasolu vormi avastamine. Nutikate nanomaterjalide tüübid: biomimeetilised, biolagunevad, ferrofluidsed, tarkvara- ja riistvarakompleksid.
esitlus, lisatud 12.08.2015
Süsiniku koht keemiliste elementide tabelis: aatomi struktuur, energiatasemed, oksüdatsiooniaste. Süsiniku keemilised omadused. Teemant, grafiit, fullereen. Adsorptsioon kui süsiniku oluline omadus. Gaasimaski ja söefiltrite leiutamine.
esitlus, lisatud 17.03.2011
Süsinikuühendite mitmekesisus, levik looduses ja kasutusala. allotroopsed modifikatsioonid. Vaba süsinikuaatomi füüsikalised omadused ja struktuur. Süsiniku keemilised omadused. Karbonaadid ja süsivesinikud. Teemandi ja grafiidi struktuur.
fullereenid selle mõiste kõige üldisemas tähenduses võib nimetada eksperimentaalselt saadud ja hüpoteetilisi molekule, mis koosnevad eranditult süsinikuaatomitest ja millel on kumera hulktahuka kuju. Süsinikuaatomid asuvad nende tippudes ja piki servi kulgevad C-C sidemed.
Fullereen on süsiniku molekulaarne vorm. Levinud määratlus on see fullereenid, mis on tahkes olekus, nimetatakse fulleriidid. Fulleriidi kristallstruktuur on fullereeni molekulide perioodiline võre ja kristallilises fulleriidis moodustavad fullereeni molekulid fcc võre.
Fullereen on pakkunud huvi astronoomia, füüsika, bioloogia, keemia, geoloogia ja muude teaduste vastu alates üheksakümnendate aastate algusest. Fullereenile omistatakse fantastilisi raviomadusi: näiteks on fullereeni väidetavalt juba hakatud kasutama kosmeetikas noorendava vahendina kosmetoloogias. Fullereeni abil hakkavad nad võitlema vähi, HIV-i ja muude kohutavate haigustega. Samas ei võimalda nende andmete uudsus, vähene uurimus ja tänapäevase inforuumi eripära veel sellist fullereeni puudutavat infot sada protsenti usaldada.
ICM (www.veebisait)
Levinud on oluliselt lihtsustatud seisukoht, et enne fullereeni avastamist eksisteeris kaks süsiniku polümorfset modifikatsiooni – grafiit ja teemant ning pärast 1990. aastat lisati neile veel üks süsiniku allotroopne vorm. Tegelikult see nii ei ole, sest süsiniku olemasolu vormid on üllatavalt mitmekesised (vt artiklit). 
Fullereenide avastamise ajalugu
Autorirühm eesotsas L.N. Sidorova võttis monograafias "Fullerenes" kokku suure hulga selleteemalisi töid, ehkki sugugi mitte kõik: raamatu ilmumise ajaks ulatus fullereenidele pühendatud väljaannete koguarv umbes 15 tuhandeni. Autorite sõnul fullereenide avastamine– süsiniku – meie planeedi ühe levinuima elemendi – uut eksisteerimisvormi peetakse üheks 20. sajandi teaduse olulisemaks avastuseks. Vaatamata süsinikuaatomite ammutuntud ainulaadsele võimele siduda keerulisi hargnenud ja mahukaid molekulaarstruktuure, mis on kogu orgaanilise keemia aluseks, osutus siiski ootamatuks võimalus moodustada stabiilseid karkassimolekule ainult ühest süsinikust. Andmete järgi saadi 1985. aastal eksperimentaalne kinnitus, et seda tüüpi 60 ja enama aatomiga molekulid võivad tekkida looduses looduslikult toimuvate protsesside käigus, kuid ammu enne seda eeldati juba suletud süsiniksfääriga molekulide stabiilsust. .
Fullereeni tuvastamine otseselt seotud süsiniku sublimatsiooni ja kondenseerumise protsesside uurimisega.
 Uus etapp sisse fullereenid tuli aastal 1990, mil töötati välja meetod uute ühendite saamiseks grammides ja kirjeldati meetodit fullereenide eraldamiseks puhtal kujul. Pärast seda tehti kindlaks C60 fullereeni olulisemad struktuursed ja füüsikalis-keemilised omadused. C60 isomeer (buckminsterfullereen) on teadaolevate fullereenide seas kõige kergemini moodustuv ühend. Fullerene C60 sai oma nime futuristliku arhitekti Richard Buckminster Fulleri auks, kes lõi struktuure, mille kuppelraam koosnes viisnurkadest ja kuusnurkadest. Samas tekkis uurimistöö käigus vajadus üldistava nimetuse järele fullereenid suletud pinnaga (süsinikkarkass) mahuliste struktuuride jaoks nende mitmekesisuse tõttu.
Uus etapp sisse fullereenid tuli aastal 1990, mil töötati välja meetod uute ühendite saamiseks grammides ja kirjeldati meetodit fullereenide eraldamiseks puhtal kujul. Pärast seda tehti kindlaks C60 fullereeni olulisemad struktuursed ja füüsikalis-keemilised omadused. C60 isomeer (buckminsterfullereen) on teadaolevate fullereenide seas kõige kergemini moodustuv ühend. Fullerene C60 sai oma nime futuristliku arhitekti Richard Buckminster Fulleri auks, kes lõi struktuure, mille kuppelraam koosnes viisnurkadest ja kuusnurkadest. Samas tekkis uurimistöö käigus vajadus üldistava nimetuse järele fullereenid suletud pinnaga (süsinikkarkass) mahuliste struktuuride jaoks nende mitmekesisuse tõttu.
Samuti väärib märkimist, et Buckminster Fulleri järgi on nime saanud terve rida süsinikmaterjale: c60 fullereeni (buckminster fullerene) nimetatakse ka buckyballiks (Buckminster Fullerile ei meeldinud nimi "Buckminster" ja eelistas lühendatud nime "Bucky"). Lisaks nimetatakse mõnikord sama eesliitega ka süsiniknanotorusid – buckityubes, munakujulisi fullereene – buckyegg (buckyball egg) jne.
ICM (www.veebisait)
Fullereenide omadused. fulleriit
Fullereeni omadused objektiivsetel põhjustel ebapiisavalt uuritud: suhteliselt väikesel arvul laboritel on võimalus neid omadusi uurida. Kuid perioodilises ja populaarteaduslikus ajakirjanduses pööratakse fullereenidele ja nende omadustele nii palju tähelepanu... Tihtipeale levib kontrollimata informatsioon fullereenide imeliste omaduste kohta hämmastava kiirusega ja tohutul hulgal, mille tulemusena on nõrk hääl. keeldumiste kohta jääb kuulmata. Näiteks ühe teadlaste rühma väidet, et šungiidis on fullereene, on korduvalt kontrollitud, kuid see pole leidnud kinnitust (vt arutelu). Sellest hoolimata peetakse šungiiti tänapäeval "looduslikuks nanotehnoloogiliseks fullereeni sisaldavaks materjaliks" – väide, mis on minu arvates pigem turundustrikk.
Mõned teadlased väidavad, et fullereenidel on selline murettekitav omadus nagu toksilisus.
Tavaliselt, kui räägitakse fullereenide omadused tähendavad nende kristalset vormi - fulleriite.
Märkimisväärne erinevus fullereeni kristallid paljude teiste orgaaniliste ainete molekulaarsetest kristallidest, kuna nad ei suuda seda jälgida vedel faas. Võib-olla on see tingitud asjaolust, et temperatuur on 1200 Küleminek vedelasse olekusse, mis omistatakse C 60 fulleriidile, ületab juba selle väärtuse, mille juures toimub fullereeni molekulide endi süsinikskeleti märgatav hävimine.
Vastavalt andmetele, fullereenide omadused Anomaalselt kõrge stabiilsus, mida tõendavad fullereene hõlmavate protsesside uuringute tulemused, on üks neist. Eelkõige märgib autor seda kristalne fullereen eksisteerib stabiilse ainena kuni temperatuurini 1000–1200 K, mis on seletatav selle kineetilise stabiilsusega. Tõsi, see puudutab C60 fullereeni molekuli stabiilsust inertses argooni atmosfääris ning hapniku juuresolekul täheldatakse juba 500 K juures märkimisväärset oksüdatsiooni CO ja CO 2 tekkega.
Töö on pühendatud C60 ja C70 fulleriitide elektrofüüsikaliste ja termodünaamiliste omaduste põhjalikule uuringule äärmusliku šokikoormuse tingimustes.
Igal juhul tuleb fullereenide omaduste üle arutledes täpsustada, millist ühendit mõeldakse - C20, C60, C70 või mõnda muud, loomulikult on nende fullereenide omadused täiesti erinevad.
Praegu fullereenid С60, С70 ja fullereeni sisaldavaid tooteid toodavad ja pakuvad müügiks erinevad välis- ja kodumaised ettevõtted, seetõttu osta fullereene ja olge hõivatud uurides fullereenide omadusi teoreetiliselt võib igaüks. Fullereene C60 ja C70 pakutakse hinnaga, mis jääb vahemikku 15–210 dollarit grammi kohta ja rohkemgi, olenevalt tüübist, puhtusest, kogusest ja muudest teguritest. Fullereenide tootmine ja müük »
Fullereenid malmis ja terases
Eeldades olemasolu fullereenid ja fullereeni struktuurid raua-süsinik sulamites, siis peaksid need oluliselt mõjutama terase ja malmi füüsikalisi ja mehaanilisi omadusi, osaledes struktuuri- ja faasimuutustes.
ICM (www.veebisait)
Nende protsesside uurijad on pikka aega pööranud suurt tähelepanu raua-süsiniku sulamite kristalliseerumismehhanismidele. Artiklis käsitletakse ülitugevas malmis nodulaarse grafiidi moodustumise võimalikke mehhanisme ja selle struktuuri iseärasusi, võttes lihtsalt arvesse raua-süsiniku sulamite fullereenne olemus. Autor kirjutab, et "fullereenide ja fullereenidel põhinevate struktuuride avastamisega on mitmetes töödes püütud selgitada nende struktuuride põhjal sõlmelise grafiidi tekkemehhanismi."
Töös käsitletakse saavutusi fullereeni keemia vallas ja üldistatakse "uusi ideid raud-süsiniksulamite struktuuri kohta". Autor väidab, et süsiniku molekulaarne vorm on fullereenid С60- tuvastas ta klassikalise metallurgia meetoditega sulatatud raua-süsiniksulamites ning paljastab ka kolm võimalikku välimuse mehhanismi fullereenid terase ja malmi struktuuris:
Omal ajal, 5 aastat tagasi, valisime fullereen ja kuusnurk saidi www.site logona, viimaste saavutuste sümbolina raua-süsiniku sulamite uurimise vallas, uute arengute ja avastuste sümbolina, mis on seotud Fe-C sulatite muutmisega - an kaasaegse valukoja ja väikemetallurgia lahutamatu etapp.
Lit.:
Süsiniku molekulaarne vorm või selle allotroopne modifikatsioon fullereen on pikk rida aatomiklastreid C n (n > 20), mis on kumerad suletud polüeedrid, mis on ehitatud süsinikuaatomitest ja millel on viis- või kuusnurksed pinnad (siin on väga harvad erandid) . Asendamata fullereenide süsinikuaatomid kipuvad olema sp 2 -hübriidses olekus koordinatsiooninumbriga 3. Seega moodustub valentssidemete teooria kohaselt sfääriline konjugeeritud küllastumata süsteem.
üldkirjeldus
Termodünaamiliselt kõige stabiilsem süsiniku vorm tavatingimustes on grafiit, mis näeb välja nagu grafeenilehtede virn, mis on vaevu üksteisega ühendatud: kuusnurksete rakkude lamedad võred, mille ülaosas on süsinikuaatomid. Igaüks neist on seotud kolme naaberaatomiga ja neljas valentselektron moodustab pi süsteemi. See tähendab, et fullereen on just selline molekulaarne vorm, st sp 2 hübriidseisundi pilt on ilmne. Kui grafeenilehele tuuakse sisse geomeetrilisi defekte, tekib paratamatult suletud struktuur. Näiteks on sellised defektid viieliikmelised tsüklid (viisnurksed tahud), mis on süsiniku keemias sama levinud kui kuusnurksed.

Loodus ja tehnika
Fullereenide saamine puhtal kujul on võimalik kunstliku sünteesi teel. Neid ühendeid uuritakse erinevates riikides jätkuvalt intensiivselt, määrates kindlaks nende tekketingimused, samuti vaadeldakse fullereenide struktuuri ja omadusi. Nende rakendusala laieneb. Selgus, et märkimisväärne kogus fullereene sisaldub tahmas, mis tekib grafiitelektroodidel kaarelahendusel. Varem ei näinud seda fakti lihtsalt keegi.
Kui fullereene laboris saadi, hakati looduses leiduma süsiniku molekule. Karjalas leiti neid šungiitide proovidest, Indias ja USA-s - furulgiitidest. Ka meteoriitides ja põhjasetetes leidub palju ja sagedasi süsiniku molekule, mis on vähemalt kuuskümmend viis miljonit aastat vanad. Maal võivad puhtad fullereenid tekkida äikeselahenduse ja maagaasi põlemise käigus. Vahemerd üle võetud uuriti 2011. aastal ja selgus, et kõigis võetud proovides – Istanbulist Barcelonani – on fullereen. Selle aine füüsikalised omadused põhjustavad spontaanset moodustumist. Samuti on seda kosmosest leitud tohututes kogustes – nii gaasilisel kui tahkel kujul.
Süntees
Esimesed katsed fullereenide eraldamisel toimusid grafiidi kondenseerunud aurude kaudu, mis saadi tahkete grafiidiproovide laserkiirgusega. Saadi ainult fullereenide jäljed. Alles 1990. aastal töötasid keemikud Huffman, Lamb ja Kretchmer välja uue meetodi fullereenide ekstraheerimiseks grammides. See seisnes grafiitelektroodide põletamises elektrikaarega heeliumi atmosfääris ja madalal rõhul. Anood oli erodeeritud ja kambri seintele ilmus fullereene sisaldav tahm.
Järgmisena lahustati tahm tolueenis või benseenis ning saadud lahuses eraldati puhtad grammid C70 ja C60 molekule. Suhe on 1:3. Lisaks sisaldas lahus ka kaks protsenti kõrgemat järku raskeid fullereene. Nüüd oli asi väike: valida aurustamiseks optimaalsed parameetrid - atmosfääri koostis, rõhk, elektroodi läbimõõt, vool ja nii edasi, et saavutada fullereenide suurim saagis. Need moodustasid kuni umbes kaksteist protsenti tegelikust anoodimaterjalist. Seetõttu on fullereenid nii kallid.

Tootmine
Kõik eksperimentaalteadlaste katsed olid alguses asjatud: produktiivseid ja odavaid viise fullereenide saamiseks ei leitud. Ei süsivesinike leegis põletamine ega keemiline süntees ei toonud edu. Elektrikaare meetod jäi kõige produktiivsemaks, võimaldades saada umbes ühe grammi fullereene tunnis. Mitsubishi on rajanud tööstusliku tootmise süsivesinike põletamise teel, kuid nende fullereenid ei ole puhtad – need sisaldavad hapnikumolekule. Ja selle aine moodustumise mehhanism jääb endiselt ebaselgeks, kuna kaarepõlemisprotsessid on termodünaamilisest vaatepunktist äärmiselt ebastabiilsed ja see aeglustab oluliselt teooria käsitlemist. Vaid faktid, et fullereen kogub üksikuid süsinikuaatomeid, st C2-fragmente, on ümberlükkamatud. Selget pilti selle aine tekkest pole aga kujunenud.
Fullereenide kõrget hinda ei määra mitte ainult madal saagis põlemisel. Erinevate masside fullereenide eraldamine, puhastamine ja eraldamine tahmast - kõik need protsessid on üsna keerulised. See kehtib eriti segu eraldamise kohta üksikuteks molekulaarseteks fraktsioonideks, mis viiakse läbi vedelikkromatograafia abil kolonnidel ja kõrge rõhu all. Viimases etapis eemaldatakse lahustijäägid juba tahkest fullereenist. Selleks hoitakse proovi dünaamilises vaakumis temperatuuril kuni kakssada viiskümmend kraadi. Kuid eeliseks on see, et C 60 fullereeni väljatöötamise ja selle makrokogustes tootmise käigus kasvas orgaaniline keemia iseseisvaks haruks - fullereenide keemiaks, mis sai uskumatult populaarseks.
Kasu
Fullereeni derivaate kasutatakse erinevates tehnoloogiavaldkondades. Fullereenkiled ja -kristallid on pooljuhid, millel on optilise kiirguse korral fotojuhtivus. Leelismetalli aatomitega legeeritud C60 kristallid lähevad ülijuhtivusseisundisse. Fullereeni lahused on mittelineaarsete optiliste omadustega, seetõttu saab neid kasutada optiliste aknaluukide aluseks, mis on vajalikud kaitseks intensiivse kiirguse eest. Fullereeni kasutatakse ka teemantide sünteesi katalüsaatorina. Fullereene kasutatakse laialdaselt bioloogias ja meditsiinis. Siin toimivad nende molekulide kolm omadust: lipofiilsus, mis määrab membranotroopia, elektronide puudulikkus, mis annab võimaluse suhelda vabade radikaalidega, samuti võime viia oma ergastatud olek üle tavalise hapniku molekulile ja muuta see hapnik hapnikuks. singlett.
Sellised aine aktiivsed vormid ründavad biomolekule: nukleiinhappeid, valke, lipiide. Reaktiivseid hapniku liike kasutatakse fotodünaamilises ravis vähi raviks. Patsiendi verre süstitakse fotosensibilisaatoreid, mis tekitavad reaktiivseid hapniku liike – fullereene ise või nende derivaate. Kasvaja verevool on nõrgem kui tervetes kudedes ja seetõttu kogunevad sellesse fotosensibilisaatorid ning pärast suunatud kiiritamist ergastatakse molekulid, tekitades reaktiivseid hapniku liike. vähirakud läbivad apoptoosi ja kasvaja hävib. Lisaks on fullereenidel antioksüdantsed omadused ja nad püüavad kinni reaktiivsed hapnikuühendid.
Fullereen vähendab HIV integraasi, valgu, mis vastutab viiruse DNA-sse kinnistamise, sellega suhtlemise, konformatsiooni muutmise ja peamise kahjurifunktsiooni võtmise eest, aktiivsust. Mõned fullereeni derivaadid interakteeruvad otseselt DNA-ga ja takistavad restriktaaside toimet.

Veel meditsiinist
2007. aastal hakati vees lahustuvaid fullereene kasutama allergiavastaste ainetena. Uuringud viidi läbi inimese rakkude ja verega, mis puutusid kokku fullereeni derivaatidega - C60(NEt)x ja C60(OH)x. Elusorganismidega – hiirtega – tehtud katsetes olid tulemused positiivsed.
Ka praegu kasutatakse seda ainet ravimite kohaletoimetamise vektorina, kuna fullereenidega vesi (pidage meeles C 60 hüdrofoobsust) tungib rakumembraanist väga kergesti läbi. Näiteks otse verre süstitud erütropoetiin laguneb olulisel määral ja kui seda kasutada koos fullereenidega, suureneb kontsentratsioon enam kui kahekordseks ja seetõttu satub see rakku.
5.1 Füüsikalised ja keemilised omadused
Fullerene C60 on must peenkristalliline pulber, lõhnatu. C60 fullereeni tihedus on 1,65 g/cm3, mis on palju väiksem kui grafiidil (2,3 g/cm3) ja teemandil (3,5 g/cm3). See on tingitud asjaolust, et molekulid on õõnsad.
Polaarsetes lahustites (vesi, etanool, atsetoon) praktiliselt ei lahustu; lahustub hästi benseenis, tolueenis, fenüülkloriidis. Süsiniksidemete pikkused molekulis on 0,143 ja 0,139 nm ning sisemise õõnsuse läbimõõt 0,714 nm, mis soosib teise aatomi või molekuli – "külalise" - kaasamist õõnsusse. C60 säilitab oma termilise stabiilsuse kuni 1700K. Üksiku molekuli mahtmoodul on teoreetiliselt 720–900 GPa. C60 moodustumise entalpia on? 42,5 kJ/mol (võrdluseks: grafiidi tekkeentalpia on 0 kJ/mol ja teemandil 1,67 kJ/mol).
Kristallvõre C 60 on näokeskne kuup, igal molekulil on 12 "naabrit", molekulid on omavahel nõrgalt seotud. Sellist molekulaarvõret iseloomustavad madalad sublimatsioonitemperatuurid (800 °C) ja C 60 molekulid lähevad aurudesse. mis täiuslikult "elavad" gaasifaasis kuni temperatuurini 1500 K.
Fullereeni molekulidest koosnevaid kondenseerunud süsteeme nimetatakse fulleriitideks. Seda tüüpi enim uuritud süsteem on C 60 kristall ja vähem uuritud on kristalliline C 70 süsteem. Fullerite C60 on sinepivärvi tahke aine. C70 on punakaspruun tahke aine.
C60 proovid on hapniku puudumisel tundlikud ultraviolettkiirguse suhtes ja võivad osaleda lagunemisreaktsioonides. Seetõttu tuleks neid hoida pimedas ja vaakumis või lämmastiku all. Puhas fullereen toatemperatuuril on väga madala juhtivusega isolaator või pooljuht. Fullereeni molekulidel on kõrge elektronegatiivsus ja nad on võimelised enda külge kinnitama kuni kuus vaba elektroni.
Temperatuuri tõusuga kaasneb C 60 molekuli kuju kaotus. Fullereen on väljendunud elektroniaktseptor ja suudab tugevate redutseerivate ainete (leelismetallid) toimel vastu võtta kuni kuus elektroni, moodustades C 60 6- aniooni. Lisaks seob see kergesti nukleofiile ja vabu radikaale.
Fullereeni keemilised omadused on näidatud joonisel 7. Fullereen hüdrogeenitakse C 60 H 36-ks (reaktsioon 1), halogeenitakse nagu olefiinid (reaktsioonid 2, 3). Halogeenimisproduktid sisenevad kergesti nukleofiilsetesse asendusreaktsioonidesse (reaktsioon 4). Hapnikuga oksüdeerimisel (UV-kiirguse all) tekib fullereenoksiid (reaktsioon 5). Sellega seoses soovitatakse fullereeni lahuseid orgaanilistes lahustites hoida ja käidelda inertses atmosfääris. Fullereen arüülitakse AlCl3 juuresolekul (reaktsioon 6). Eespool käsitletud osmiumoksiidi lisamine on sisuliselt oksüdatsioon, mis toimub läbi avaneva kaksiksideme (reaktsioon 7). Fullereeni kaksiksidemete avanemisega liituvad ka amiinid (reaktsioon 8), aminohapped (reaktsioon 9) ja tsüaniidid (reaktsioon 10). Mitut aminorühma sisaldav fullereen on vees lahustuv. Leelismetallidega (näiteks tseesiumi või rubiidiumiga) redutseerimisel kandub elektron metalliaatomilt fullereeni. Saadud ühenditel on ülijuhtivus madalal temperatuuril, ülijuhtivuse ilmnemise kriitiline temperatuur on 33 K.
fullereeni keemilise sorptsiooni nanostruktuur
Joonis 7 – Fullereeni keemilised omadused
Polütsüleen, selle omadused ja omadused
Polüatsetüleeni tihedus = 0,04-1,1 g/cm, kristallilisusaste 0-95%. Polüatsetüleeni cis- ja trans-vormid on tuntud; cis-vorm laadimisel. kuni 100-1500C läheb transformatsioonivormi. Polüatsetüleen ei lahustu üheski tuntud orgaanilises lahustis...
Kaadmiumi kristallvõre on kuusnurkne, a = 2,97311, c = 5,60694 (temperatuuril 25 °C); aatomiraadius 1,56, ioonraadius Cd2+ 1,03. Tihedus 8,65 g/cm3 (20 °C), st 320,9? C, tkip 767 °C, soojuspaisumise koefitsient 29,8×10-6 (temperatuuril 25 °C); soojusjuhtivus (0 oC juures) 97...
Tsinkfosfaadi saamine
Elavhõbe on ainus metall, mis on toatemperatuuril vedel. Tahke elavhõbe kristalliseerub rombilisteks süngooniateks, a = 3,463, c = 6,706; tahke elavhõbeda tihedus 14,193 g/cm3 (-38,9 °C), vedel elavhõbe 13,52 g/cm3 (20 °C), aatomiraadius 1,57, ioonraadius Hg2+ 1,10; tpl - 38...
Isokinoliini derivaatide (papaveriinvesinikkloriid) farmatseutiline analüüs
Papaveriinvesinikkloriid on valge kristalne pulber kergelt mõru maitsega, lõhnatu. Sulamistemperatuur - 225ºС. See lahustub hästi vees, halvasti - etüülalkoholis, kloroformis, dietüüleetris ...
Püridiini derivaatide (nikotiinhape) farmatseutiline analüüs
Puhas nikotiinhape on värvitud nõelakujulised kristallid, mis lahustuvad kergesti vees ja alkoholis. See on termostabiilne ja säilitab oma bioloogilise aktiivsuse ka keetmisel ja autoklaavimisel...
Furaani derivaatide (furagin) farmatseutiline analüüs
Furagin on värvitu kristalne pulber sulamistemperatuuriga 85 °C ja keemistemperatuuriga 32 °C. Molekulmass (amu): 68,07. Furaanil on atsidofoobsed omadused. Kontsentreeritud väävelhappe toimel polümeriseerub ...
Joodi ja selle ühendite füüsikalis-keemilised omadused
Jood lahustub vees vähe. Toatemperatuuril lahustub 100 g vees umbes 0,03 g joodi, temperatuuri tõustes joodi lahustuvus veidi suureneb. Jood lahustub palju paremini orgaanilistes lahustites...
Fullereenide keemia
Fullerene C60 on must peenkristalliline pulber, lõhnatu. C60 fullereeni tihedus on 1,65 g/cm3, mis on palju väiksem kui grafiidil (2,3 g/cm3) ja teemandil (3,5 g/cm3). See on tingitud asjaolust, et molekulid on õõnsad ...
leelismetallid
Leelismetallide kõrge keemilise aktiivsuse tõttu vee, hapniku ja mõnikord isegi lämmastiku (Li, Cs) suhtes hoitakse neid petrooleumikihi all. Leelismetalliga reageerimiseks...
Fullereen on molekul, mis on kuuekümnest süsinikuaatomist koosnev suletud kera. 2010. aastal, seoses fullereeni avastamise 25. aastapäevaga, see Doodle otsingumootor Google. Nüüd on esimene aruanne C60 sünteesi kohta rohkem kui 30 aastat vana ja selle avastamise ajalugu krooniv Nobeli preemia on veidi vähem kui 20 aastat vana, samas kui fullereeni uurimine ise alles käib. Miks on see molekul nii huvitatud teadlastest üle kogu maailma? Miks paljud inimesed, kes ei ole teadusega väga kursis, sellest vähemalt midagi kuulsid?
Alustame sissejuhatusega C60 ajaloost. Tihti eelnevad tähelepanuväärsele avastusele sündmused, millel esmapilgul sellega otsest seost ei ole, kuid tähelepanelikult vaadates ühendavad need tingimata mitme targa inimese kohtumise, huvitava idee ja värsked katsetulemused, mis võimaldavad võtta uus pilk huvipakkuvale probleemile.
Kõik sai alguse sellest, et 1970. aastate keskel avastas Harold Kroto kosmose spektriandmete põhjal pikad süsiniku molekulaarahelad ja tal tekkis soov neid laboris hankida. 1980. aastate alguses töötati välismaal Rice'i ülikoolis (Texas, USA) Richard Smalley laboris välja seadmed tulekindlatest elementidest moodustunud ühendite ja klastrite uurimiseks.
Jääb need kaks sündmust omavahel ühendada. Seda tegi Nobeli meeskonna kolmas liige Robert Curle, kes külalisena Sussexi ülikooli Kroto laboris kutsus ta külastama Smalley laborit, mida ta tegi 1984. aastal. Krotole avaldas muljet seadistuse teostatavus ja ta soovitas asendada metallketta grafiidiga, et luua metalliklastrite asemel süsinikahelaid, simuleerides selliseid tingimusi nagu tähekestes.
1985. aasta augustis tuli Kroto Smalley’sse sellises eksperimendis osalema. Nii algas tema ajalooline 10-päevane visiit. Need 10 päeva septembris andsid 60 ja 70 süsinikuaatomiga struktuuride massispektris esimesed ebaselged piigid ning seejärel tõlgendati neid suletud struktuuridena, mis on kujundatud jalgpalli- ja ragbipalliks. Ja 13. septembril ajakirja toimetus Loodus sai artikli pealkirjaga "C60: Buckminsterfullerene". Fullereeni molekuli on selles artiklis kujutatud jalgpallipalli abil – ilmselt polnud autoritel lihtsalt aega arusaadava aatomimudeli ehitamiseks.
Miks eeldasid autorid, et saadud C60 molekul on täpselt suletud sfäär, mitte ahel? Selle põhjuseks on muuhulgas asjaolu, et loodus "armastab" sümmeetrilisi struktuure ja kärbitud ikosaeedril (jalgpallipalli kuju) on kõige suurem sümmeetria. Kroto kirjutas: "Mäletan, et mõtlesin, et see molekuli vorm on nii ilus, et see peab olema tõsi." Krotot inspireeris kuppel, mille ehitas 1983. aastal surnud väljapaistev leiutaja ja filosoof Buckminster Fuller, kelle järgi uus molekul sai nime.
![]()
Tuleb märkida, et fullereene ennustati teoreetiliselt juba ammu enne eksperimentaalset tootmist. 1966. aastal tegi David Jones ettepaneku, et viisnurksete defektide sisseviimine korrapärastest kuusnurkadest koosnevasse grafiidikihti võib muuta selle lameda kihi õõnsaks suletud struktuuriks. 1971. aastal Jaapanis arutas füüsik Osawa sellise struktuuri olemasolu võimalikkust (joonis 3). Kuid ta avaldas selle tulemuse Jaapani ajakirjas Kagaku("Keemia"), mis ilmub ainult jaapani keeles. Siis aasta hiljem kirjutas ta raamatu aromaatsusest, kuid jällegi jaapani keeles, mis sisaldas fullereeni peatükki. Keelebarjääri tõttu oli tema töö teadusringkondadele teada alles C60 eksperimentaalsest avastamisest.
Tuleb märkida, et NSV Liidus viidi 1971. aastal esimest korda läbi fullereeni stabiilsuse ja elektronstruktuuri kvantkeemiline arvutus. See juhtus järgmisel viisil. Venemaa Teaduste Akadeemia Organoelementide Ühendite Instituudi (INEOS RAS) direktor oli tollal NSVL Teaduste Akadeemia akadeemik AN Nesmejanov, ta soovitas kvantkeemia labori juhatajal DA Bochvaril uurida õõnsaid süsiniku suletud struktuure. millesse saab paigutada metalliaatomeid ja seeläbi isoleerida need keskkonnast.
Koos oma kolleegide E. G. Galperni ja I. V. Stankevitšiga alustas seda tööd D. A. Bochvar. See algas dodekaeedri kujuga C20 molekuli stabiilsuse uurimisega, seetõttu nimetati seda karbododekaeedriks. Sellise molekuli suurus on aga väike, mis esialgu piirab võimalust sinna metalliaatomeid sisestada. Ja mis kõige tähtsam, arvutustulemused näitasid, et selline struktuur peab olema ebastabiilne. Töö on seisma jäänud. I. V. Stankevitš, kes oli innukas jalgpallur, pakkus välja veel ühe võimaliku C60 süsinikust suletud konstruktsiooni, millel on kärbitud ikosaeedri sümmeetria – jalgpallipall. Ta tõi laborisse jalgpallipalli ja ütles Galpernile: "Lena, 22 tervet meest peksavad seda palli tunde ja sellega ei tehta midagi. Sellise kujuga molekul peab olema väga tugev.

Sellise suurusega molekuli kvantkeemiline arvutamine oli tollaste arvutite jaoks väga keeruline, kuid see viidi läbi ja näitas, et C60 on stabiilne molekul. Alguses ei suutnud Bochvar, Halpern ja Stankevitš keemikuid veenda sellise molekuli olemasolus ning alles 1972. aastal ilmus Ameerika teadlaste lühike märkus võimaliku C20 dodekaeedri molekuli kohta, millega autorid pöördusid AN-i. Nesmeyanov ajendas teda esitama töö C60 kohta Doklady AN SSSRis. Kahjuks ei õnnestunud Bochvaril, Halpernil ja Stankevitšil veenda eksperimentaalkeemikuid seda struktuuri sünteesima ning kuni sünteesini 1985. aastal peeti seda struktuuri teoreetiliseks leiutiseks. Nobeli preemia laureaadid on märkinud oma panust C60 uurimisse. Smalley Nobeli loengus märgiti, et seda auhinda väärisid Osawa, Jones, Halpern, Stankevitš, kellest igaüks andis oma panuse avastusse.
Fullereeni avastamise ajalugu saab lõpetada Kroto sõnadega tema Nobeli loengust: „C60 avastamise ajalugu ei saa õigesti hinnata, võtmata arvesse selle molekuli kuju ilu, mis on tingitud selle molekuli kujust. uskumatu sümmeetria. Teine oluline fakt, mis selle molekuli ümber aura loob, on seotud selle nimega – buckminsterfullereen. Kõik see annab meie elegantsele molekulile karisma, mis on paelunud teadlasi, rõõmustanud elanikke, lisanud noortele entusiasmi suhtumises teadusesse ja andnud eelkõige värske hingamise keemiale.
Fullereeni ja fulleriidi omadused
Puhas fullereen toatemperatuuril on umbes 2 eV ribalaiusega isolaator või väga madala juhtivusega sisemine pooljuht. On teada, et tahketes ainetes võib elektronidel olla energiat ainult teatud väärtusvahemikes - lubatud energiatsoonides, mis moodustuvad aatomi- või molekulaarenergia tasemetest. Need ribad on eraldatud keelatud energiate ribadega, mida elektronidel ei saa olla.
Alumine riba on reeglina täidetud elektronidega, mis osalevad aatomite või molekulide vahelise keemilise sideme moodustamises, seetõttu nimetatakse seda sageli valentsribaks. Selle kohal asub ribapilu, millele järgneb tühi või mittetäielikult täidetud lubatud energiate riba ehk juhtivusriba. Oma nime sai see sellest, et selles on alati vabu elektroonilisi olekuid, mille tõttu saavad elektronid elektriväljas liikuda (triivida), teostades nii laenguülekannet ehk teisisõnu tagades elektrivoolu kulgemise (tahkekeha juhtivuse) .
Fullereeni kristallid (fulleriidid) on pooljuhid, mille ribavahemik on 1,2–1,9 eV ja millel on fotojuhtivus. Nähtava valgusega kiiritades fulleriidi kristalli elektritakistus väheneb. Fotojuhtivust ei oma mitte ainult puhas fulleriit, vaid ka selle erinevad segud teiste ainetega. Leiti, et kaaliumiaatomite lisamine C60 kiledele põhjustab ülijuhtivuse ilmnemist 19 K juures.
Seoses enda külge erineva keemilise olemusega radikaale, on fullereenid võimelised moodustama laia klassi erinevate füüsikalis-keemiliste omadustega keemilisi ühendeid. Nii saadi polüfullereenkiled, milles C60 molekulid on omavahel seotud mitte van der Waalsi, nagu fulleriidi kristallis, vaid keemilise interaktsiooni kaudu. Need plastiliste omadustega kiled on uut tüüpi polümeersed materjalid. Huvitavaid tulemusi on saavutatud fullereenidel põhinevate polümeeride sünteesi suunal. Sel juhul on polümeeri ahela aluseks C60 fullereen ja molekulide vaheline ühendus toimub benseenirõngaste abil. See struktuur on saanud kujundliku nime "pärlipael".
Fullereeni polümerisatsioon toob kaasa ebatavaliste efektide ilmnemise, mis on kaasaegse tehnoloogia jaoks paljulubavad. Fullereenide kombinatsioon teiste süsiniku nanostruktuuridega toob kaasa huvitavaid objekte: süsinik-nanotorude sees olevad fullereenid moodustavad "hernekaunad" ( herbujalad), mida võidakse kasutada laserites, üheelektronilistes transistorides, kvantarvutite spin-kubitites jne, samas kui elektronkiire mõju võib viia fullereeni polümerisatsioonini sisemises süsiniktorus. Teisest küljest tekitab fullereeni lisamine nanotoru pinnale paljutõotavate emissiooniomadustega "nanopunga".
V. D. Blank, M. Yu. Popov ja S. G. Buga said 1993. aastal FGBNU TISNUMis (Moskva, Troitsk) esimest korda fullereenidel põhineva uue materjali – ülikõva fulleriidi ehk tisnumiidi, millel on rekordilised elastsuskonstandid ja kõvadus ning mis võib isegi kriimustada. teemant. L. A. Chernozatonsky pakkus välja sellise polümeeri mudeli, mis langes katsega ideaalselt kokku. Selle materjali ainulaadsed omadused on ilmselt tingitud sellest, et selles sisalduv polümeriseerunud fulleriit on kokkusurutud olekus, suurendades oluliselt kogu materjali mehaanilist jäikust ja kõvadust. Seejärel saadi teistest rühmadest ülikõva süsiniku proovid.


Süsinikuvaba fullereenid
Suletud õõnesstruktuuri võivad moodustada mitte ainult süsinikuaatomid. Loomulik oleks eeldada, et boornitriid, süsiniku isoelektrooniline analoog, võib samuti moodustada sarnase kujuga molekuli. Sellised struktuurid saadi aga alles 1998. aastal ning mittesüsiniku fullereenide sarja esimesed liikmed olid suletud struktuurid koostisega MoS2 ja WS2. Need ühendid kuuluvad siirdemetallide dikalkogeniidide klassi – ühendid, mis koosnevad metalliaatomite kihtidest, mille mõlemal küljel on kalkogeeni (antud juhul väävli) kihid. Selliste fullereenide eripäraks on nende keemiline inertsus, mis võimaldab neid kasutada suurepärase määrdeainena. Ettevõtted Nanomaterjalid ja N.I.S. müüa selliseid tooteid rohkem kui 1000 tonni aastas.

Hetkel on avastatud mitukümmend mittesüsiniku fullereene, millel on erinev struktuur ja koostis. Sageli eelneb sünteesile teoreetiline ennustus, mis võimaldab hinnata materjali omadusi. Näiteks 2001. aastal pakuti välja magneesiumdiboriidist pärit fullereenide mudelid. 2007. aastal ennustas Boris Yakobsoni (Riisiülikool) rühm fullereeni, mis koosneb täielikult boor B80-st, millel on sama sümmeetria kui C60-l. Artikkel sellisest ilusast molekulist äratas teadlaskonnas suurt huvi, ennustati mitmeid erineva arvu aatomeid sisaldavaid stabiilseid boorfulereene ning 2014. aastal avaldati artikkel, milles räägiti boorfulereeni B40 edukast sünteesist. Hiljuti avaldati töö, mis ennustab C60Sc20 stabiilset struktuuri – fullereeni, milles süsinikuaatomite viieliikmelised tsüklid on omavahel seotud metalliaatomite kaudu. Selline molekul on hea stabiilsusega ja seda saab tõenäoliselt kasutada molekulaarse vesiniku sorbendina. Eksperimendi otsustada.
lisakirjandust
Croto G. Sümmeetria, ruum, tähed ja C60 // Uspekhi fizicheskikh nauk. 1998. V. 168, nr 3. S. 343.
Jones D. E.H. Ariadne // New Sci. 1966 kd. 32. Lk 245.
Osawa E. Supersümmeetria // Kagaku Kyoto. 1970 kd. 25. Lk 854.
Bochvar D. A., Galpern E. G. C20 ja C60 molekulide elektrooniline struktuur // DAN SSSR Chemical series. 1973. V. 209, nr 3. S. 610–615.
Smalley R.E. Fullereenide avastamine // Uspekhi fizicheskikh nauk. 1998. V. 168, nr 3. S. 323.
Nasibulin A.G. et al. Uudne hübriidsüsinikmaterjal // Nat. Nanotehnoloogia. 2007 kd. 2, nr 3. Lk 156–161.
Tühi V. et al. Kas C60 fulleriit on kõvem kui teemant? // Phys. Lett. A. 1994. Vol. 188, nr 3. Lk 281-286.
Chernozatonskii L.A., Serebryanaya N.R., Mavrin B.N.Ülikõva kristalne kolmemõõtmeline polümeriseeritud C60 faas // Chem. Phys. Lett. 2000 kd. 316, nr 3-4. Lk 199–204.
Chernozatonsky L.A. Bifullereenid ja binanotorud diboriididest // JETP Letters. 2001. V. 74, nr 6. S. 369–373.
Gonzalez Szwacki N., Sadrzadeh A., Yakobson B.I. B80 Fullereen: geomeetria, stabiilsuse ja elektroonilise struktuuri absoluutne ennustamine // Phys. Rev. Lett. 2007 kd. 98, nr 16. Lk 166804.
Zhai H.J. et al. Täisboori fullereeni vaatlus // Nat. Chem. 2014. Kd. 6. Lk 727–731.
Wang J., Ma H.-M., Liu Y. Sc20C60: volleyballene // Nanoskaala. 2016. aasta.